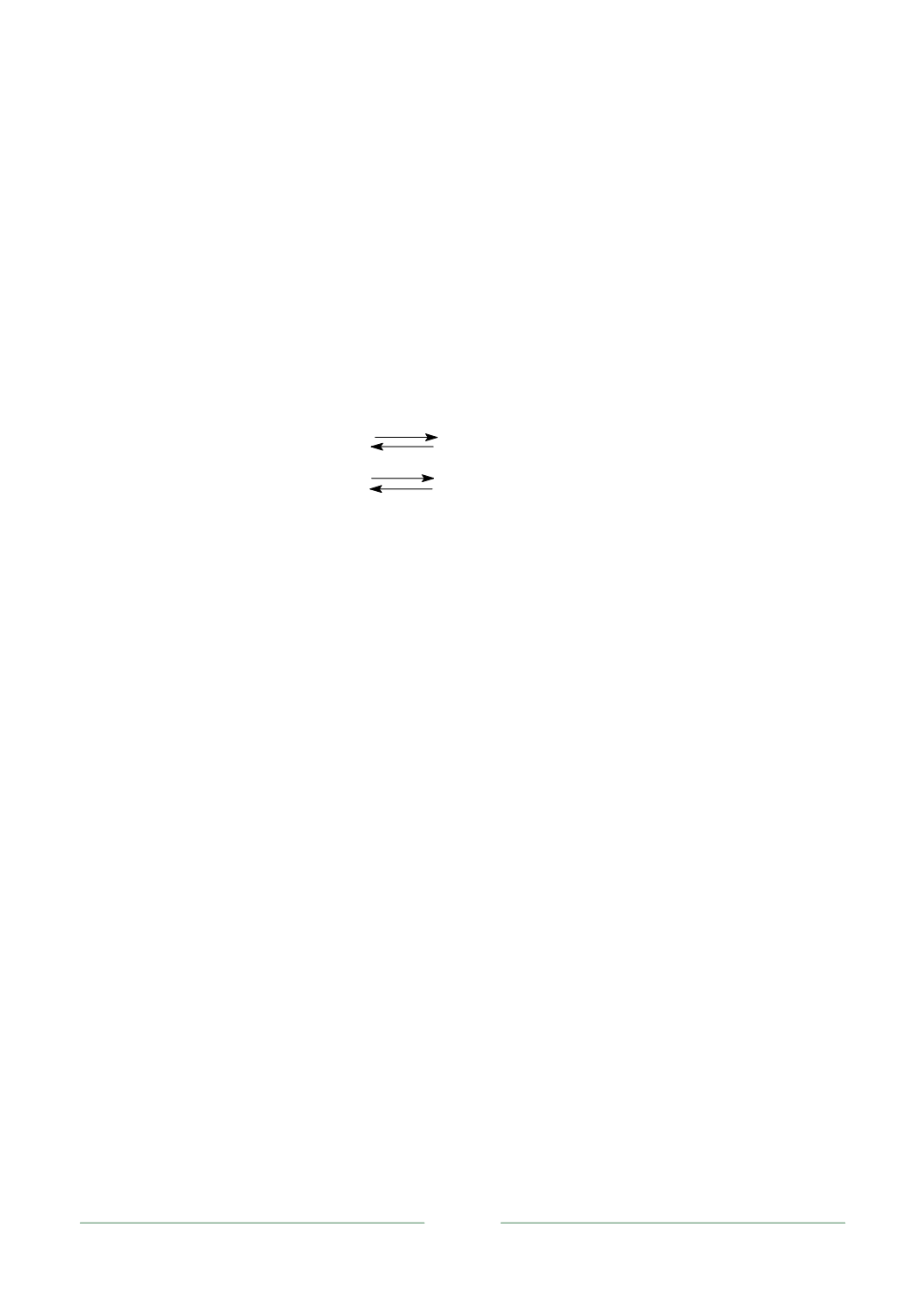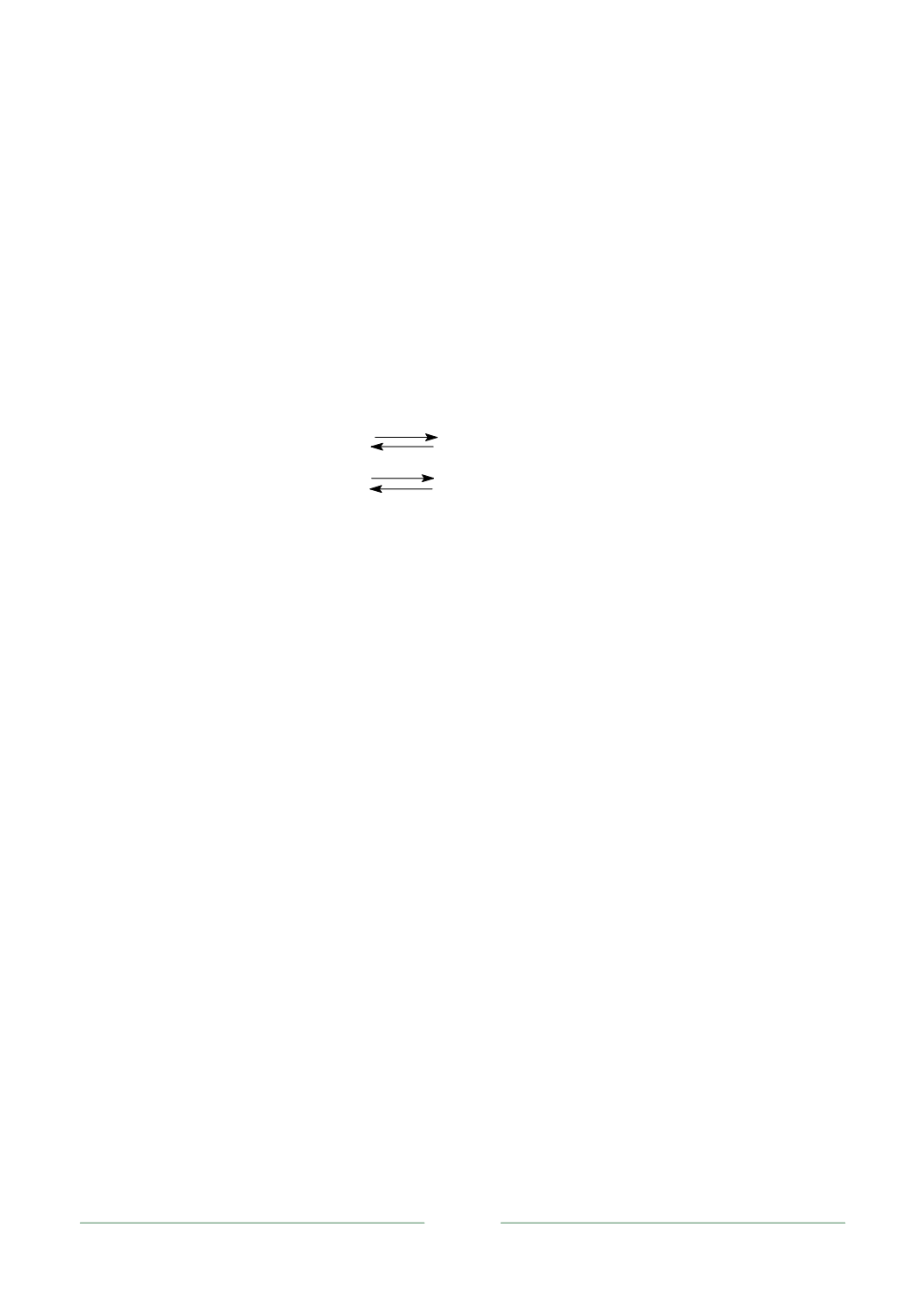
32
что приводит к образованию дисульфидных связей между белковыми молеку-
лами. Более того, ассоциаты денатурированного
β
-Лг способны осаждаться на
поверхности казеиновых мицелл, в том числе с образованием комплексов с
κ
-Кн поверхности мицеллы. Это обстоятельство приводит к изменению техно-
логических свойств молока: экранируется пептидная связь, гидролизуемая про-
теолитическим ферментом химозином (сычужным ферментом), молоко стано-
вится непригодным для сыроделия. В связи с чем молоко, предназначенное для
сыроделия, пастеризуют в щадящем режиме.
Можно отметить еще один негативный момент в поведении денатуриро-
ванных сывороточных белков, прежде всего
β
-Лг. Как отмечалось ранее, в со-
став мицеллярного казеина входит достаточно большое количество коллоидно-
го фосфата кальция. Между ортофосфорнокислыми солями кальция существу-
ют равновесия:
Во время пастеризации молока при повышении температуры равновесия
смещаются вправо, и часть гидроортофосфата и дигидроортофосфата перехо-
дит в плохорастворимый ортофосфат кальция, который может седиментировать
вместе с денатурированным
β
-Лг как на поверхности мицелл, так и на поверх-
ности технологического оборудования в виде так называемого молочного
камня.
α
-Лактальбумин – это компактный глобулярный белок, содержащий все-
го 123 аминокислотных остатка. Имеет три генетических варианта – А, В и С.
Кроме главного компонента, установлено наличие нескольких минорных, отли-
чающихся от основного электрофоретической подвижностью. Некоторые ми-
норные компоненты являются гликопротеинами.
α
-Лактальбумин содержит
ионы кальция, который включается в белок через фрагменты глутаминовой и
аспарагиновой кислот пространственно разделенных участков полипептидной
цепи по типу солевого мостика. В результате происходит стабилизация третич-
ной структуры
α
-Ла, что приводит к необычайно высокой термостабильности
белка. Так, тепловая коагуляция
α
-Ла наблюдается при температуре 114
0
С
(рН 7), в то время как температура денатурации составляет
62
0
С. Наблюдаемое противоречие связано с высокой способностью денатури-
рованного
α
-Ла к ренатурации. Третичная структура восстанавливается за счет
повторного взаимодействия ионов кальция с карбоксилатными группами аспа-
рагиновой и глутаминовой кислот денатурированного белка с восстановлением
пространственной структуры. Обратимость денатурации при рН 6-7 составляет
около 90 %.
Высокое содержание в составе
α
-лактальбумина цистеина является при-
чиной образования при температурной обработке молока серосодержащих со-
единений – сероводорода, сульфанов (сульфаны – это полисероводороды H
2
S
x
,
х
≥
2, желтые жидкости с резким запахом), метил-, диметилсульфанов, меркап-
Ca
3
(PO
4
)
2
+
CaHPO
4
Ca(H
2
PO
4
)
2
H
3
PO
4
+
3
CaHPO
4
H
3
PO
4
,