113
Fe (II),
d
6
4
s
4
p
d sp -
гибридизация
3
3
d
3
d
d sp
N N
-
N N
-
связи Fe-N
N
N
N
N
Fe
L
L
L
L
M
a
б
N (Гис)
3
N
HC
C NH
CH
CH
2
глобин
L
2
2
O
2
O
O
L
Fe (II),
d
6
Fe (II),
d
6
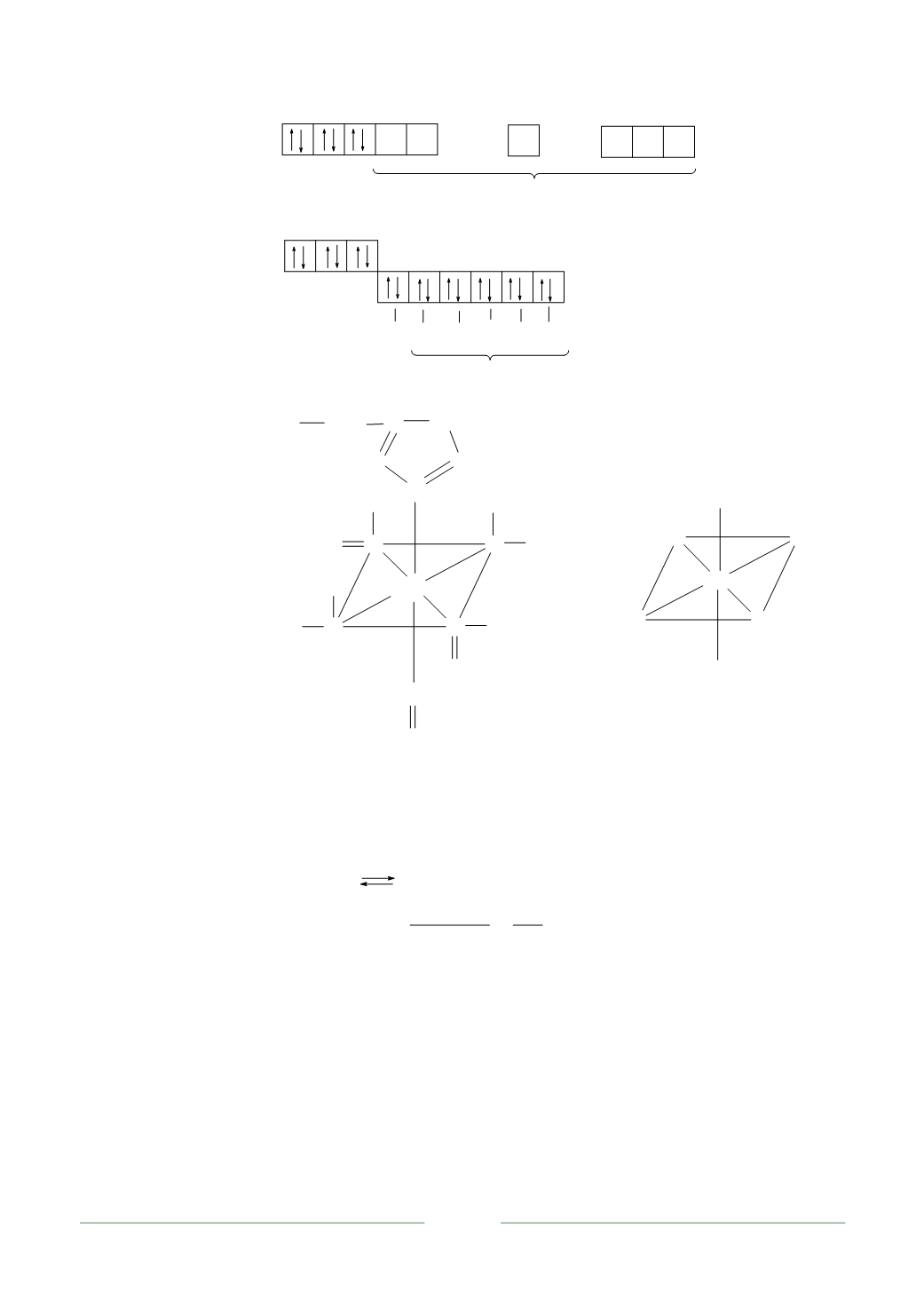
Рис. 2.5. Схема образования координационных связей:
а
– миоглобина с О
2
;
б
– в обобщенной октаэдрической структуре
Связывание кислорода с миоглобином определяется константой равнове-
сия реакции:
Mb (миоглобин) + О
2
MbО
2
, определяемой уравнением
1
1
O
2
2
]Mb [
]
MbO [
−
=
=
k
k
P
К
.
Константа скорости связывания миоглобина с кислородом равна
1,0-1,9
⋅
10
7
М
-1
⋅
с
-1
, тогда как значение
k
-1
составляет 10-70 с
-1
. Соответственно
константа равновесия имеет порядок 10
6
-10
7
. Однако при низких парциальных
давлениях кислорода, в соответствии с принципом Ле-Шателье, равновесие
смещается влево, и миоглобин переходит в дезокси-форму.
Кривая поглощения О
2
миоглобином описывается гиперболической кри-
вой, которая при увеличении давления стремится к своей предельной величине,
α
=1(100 %) (рис. 2.6). Впервые уравнение этой кривой получено А.В. Хиллом
(1910 г.).
k
1
k-
1


