М а т е р и а л ы X В с е р о с с и й с к о й н а у ч н о - п р а к т и ч е с к о й к о н ф е р е н ц и и
77
0.02 0.04 0.06 0.08 0.10
10
-3
10
-2
2
C
Ph
, ммоль/л
K(Cr), с
-1
1
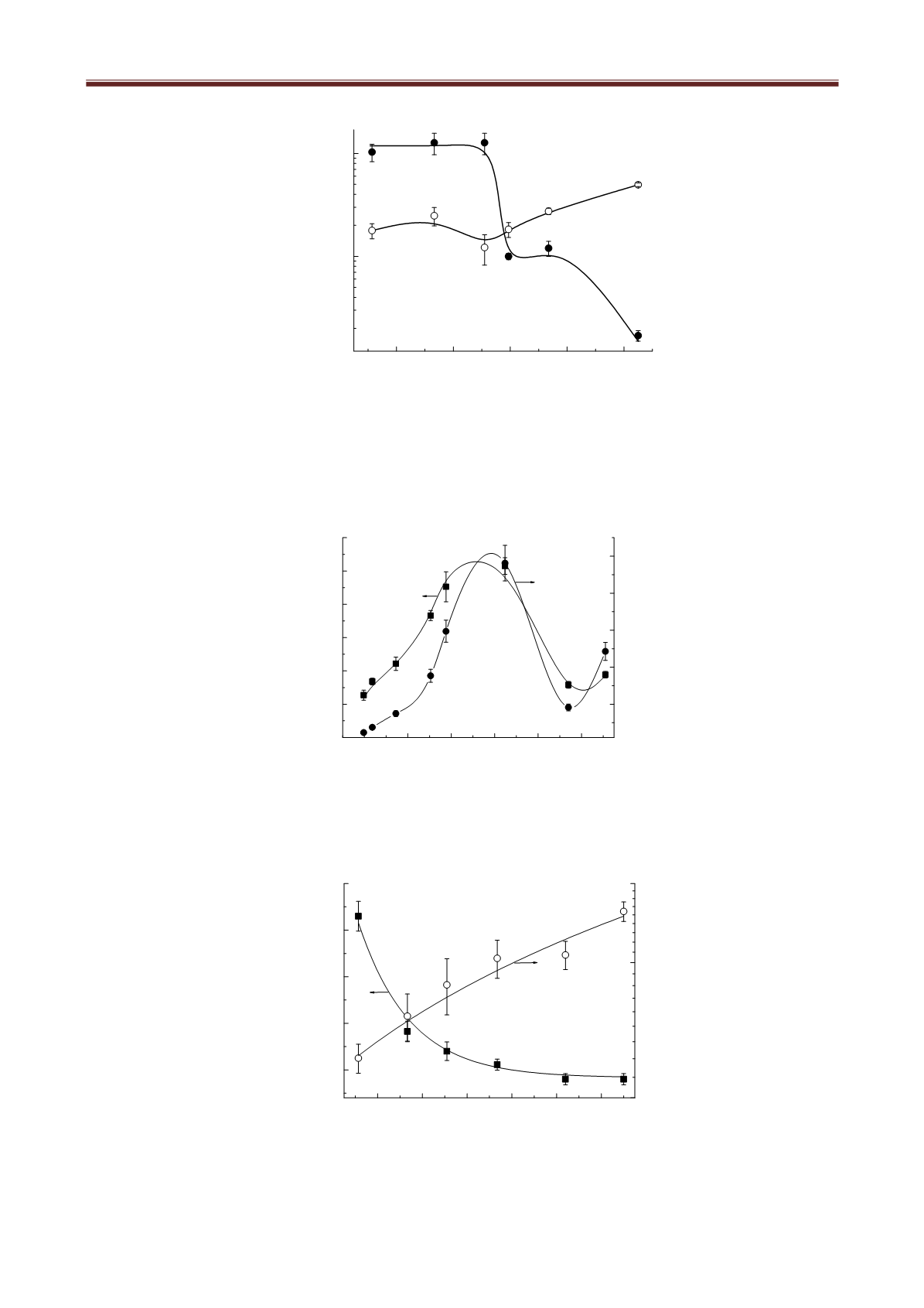
Рис. 3. Константа скорости окисления Cr
3+
(
1
) и восстановления Cr
6+
(
2
) как функция
начальной концентрации фенола. Начальная концентрация Cr
6+
-0.398 ммоль/л. Ток
разряда 40 мА.
Для этих же условий константы скорости и скорости деградации Ph
показаны на Рис. 4,5.
0.02 0.04 0.06 0.08 0.10 0.12
0.000
0.002
0.004
0.006
0.008
0.010
0.012
0.0002
0.0004
0.0006
0.0008
0.0010
W,ммоль×л
-1
×с
-1
2
K, c
-1
С(Ph), ммоль/л
1
Рис. 4. Константа скорости (
1
) и начальная скорость (
2
) разложения фенола как
функция его начальной концентрации. Ток 40 мА. Начальная концентрация Cr
6+
0.19
ммоль/л
0.02 0.04 0.06 0.08 0.10 0.12
0.005
0.010
0.015
0.020
0.025
2x10
-4
4x10
-4
6x10
-4
С
Ph
, ммоль/л
W,ммоль×л
-1
×с
-1
2
1
K, с
-1
Рис. 5. Константа скорости (
1
) и скорость разложения фенола (
2
) как функция
начальной концентрации фенола. Ток 40 мА. Начальная концентрация Cr
6+
-0.389
ммоль/л.


