Нагревательные печи и устройства
38
тер, так как в каждом из слоев можно встретить каждую из перечис-
ленных выше составляющих. Окисление железа протекает в соответст-
вии со следующими реакциями:
Fe + 0,5O
2
= FeО; 3FeО + 0,5O
2
= Fe
3
О
4
; Fe + Fe
3
O
4
= 4FeО;
2Fe
3
O
4
+ 0,5O
2
= 3Fe
2
O
3
; Fe + CO
2
= FeO + СО;
Fe + Н
2
О = FeО + Н
2
; 3FeO + СО
2
= Fe
3
O
4
+ СО;
3FeO + Н
2
О = Fe
3
O
4
+ Н
2
.
(2.1)
При окислении железа выделяется следующее количество тепла: при
образовании FeO – 4815…5003 кДж/кг; Fe
3
O
4
– 5799…6636 кДж/кг;
Fe
2
O
3
– 6365…7490 кДж/кг.
а
)
б
)
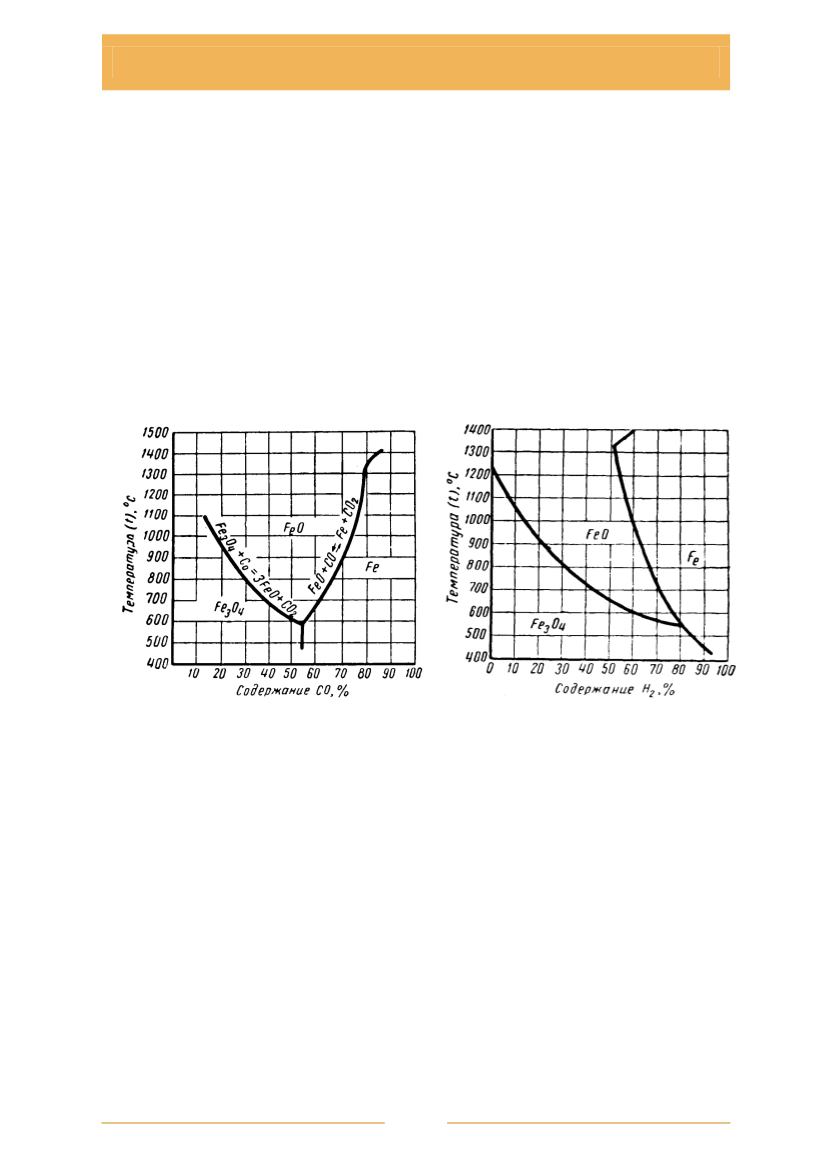
Рис. 2.2. Диаграмма равновесия реакций окисления Fe при разных температурах:
а
– равновесие CO2 – CO – Fe (Fe
3
O
4
– FeO);
б
– равновесие Н
2
О – Н
2
– FeО – Fe (Fe
2
O
3
– FeO)
Равновесие в процессе окисления железа является обратимым. В
зависимости от состава газов и температуры они могут протекать в
двух противоположных направлениях. На рис. 2.2,
а
,
б
приведены диа-
граммы равновесия реакций FeО с СО
2
и Н
2
О в зависимости от темпе-
ратуры.
Окисление при нагреве характеризуется следующими величинами:
У
=
М
1
-
М
2
;
у
= (
М
1
-
М
2
)/
τ
;
а
м
= (
М
1
-
М
2
) 100/
М
1
;
а
F
= (
М
1
-
М
2
) /
F
1
;
С
к
= (
М
1
-
М
2
) /
F
τ
,
(2.2)


